Neuartige Hochgeschwindigkeits-Ultraschallgeräte erlauben in Kombination mit einer KI-gestützten Bildanalyse hoch aufgelöste Einblicke ins Säuglings-Gehirn. Forschende der Friedrich-Alexander-Universität Erlangen-Nürnberg (FAU) wollen diese Methode weiterentwickeln und mögliche Einsatzgebiete untersuchen. In ihrem Fokus stehen dabei der Schlaganfall während oder direkt nach der Geburt sowie die sogenannte Asphyxie, ein gefährlicher Sauerstoffmangel bei Neugeborenen. Die Deutsche Gesellschaft für Ultraschall in der Medizin (DEGUM) fördert das Projekt mit knapp 180.000 Euro.
Manche Säuglinge erleiden während oder direkt nach der Geburt einen Schlaganfall. Die Diagnose erfolgt bislang meist mit einem Magnetresonanz-Tomographen (MRT). Doch die MRT-Untersuchung von Neugeborenen ist besonders herausfordernd; zudem verfügen nicht alle Krankenhäuser über ein derartiges Gerät. Die neue Ultraschall-Technologie könnte sich zumindest für eine erste schnelle Abklärung eignen und damit auch die Einleitung einer passenden Therapie beschleunigen.
Bei Neugeborenen sind die Schädelknochen noch nicht miteinander verwachsen. Dadurch ist ihr Kopf nicht starr, sondern lässt sich etwas verformen, so dass er besser durch den Geburtskanal gelangen kann. „Die unverknöcherte Region – die Fontanelle – erlaubt es uns, das Gehirn von Säuglingen per Ultraschall zu untersuchen“, erklärt PD Dr. Dr. Adrian Regensburger, Oberarzt in der Kinder- und Jugendklinik am Uniklinikum Erlangen. „Bei Erwachsenen lässt sich dagegen per Ultraschall nur sehr wenig erkennen, weil der Schädel das Gehirn abschirmt.“
Doch auch bei Säuglingen bilden normale Ultraschall-Geräte die Gefäße im Gehirn oft nicht genau genug ab, als dass die Bilder sich zur Schlaganfall-Diagnose eignen würden. Regensburger untersucht daher zusammen mit seinen Kollegen PD Dr. Dr. Ferdinand Knieling und Dr. Gregor Hanslik, ebenfalls Oberärzte in der Kinderklink des Uniklinikums, eine deutlich verbesserte Methode. Bei ihr werden den kleinen Patientinnen und Patienten einige Tropfen Kontrastmittel in die Vene injiziert. Die Flüssigkeit enthält kleine Gasbläschen, jedes so groß wie ein rotes Blutkörperchen. Sie erscheinen im Ultraschall hell.
KI verfolgt die Reise der Kontrastmittel-Bläschen durchs Gehirn
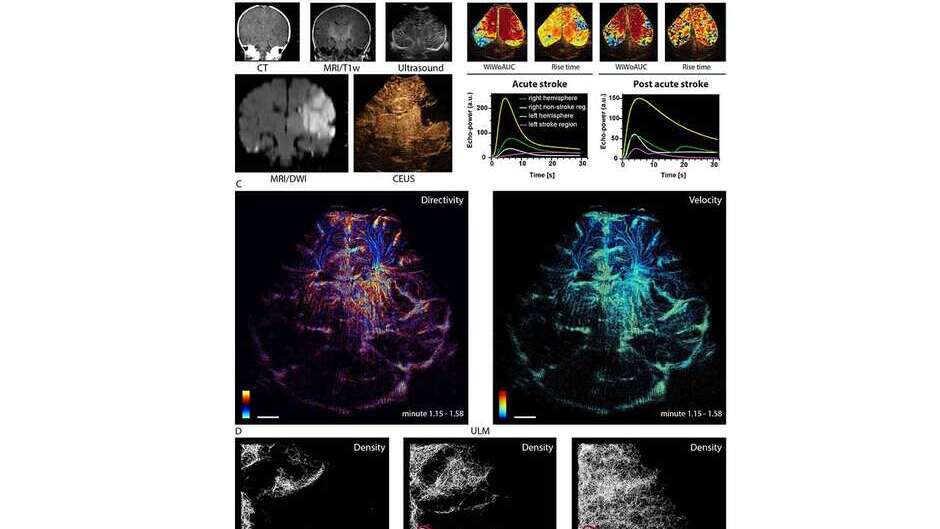
Entsprechend trainierte KI-Verfahren können im Ultraschall-Film einzelne Kontrastmittel-Bläschen erkennen und ihre Reise durch das Gehirn verfolgen. „Dadurch können wir nicht nur die Gefäße sichtbar machen, sondern auch genau analysieren, wo es Verengungen oder Blockaden gibt“, erklärt Regensburger. Um der künstlichen Intelligenz ihre Arbeit zu erleichtern, nutzen die Wissenschaftler zudem Hochgeschwindigkeits-Ultraschallgeräte. Diese zeichnen nicht wie meist üblich zwanzig Bilder pro Sekunde auf, sondern bis zu dreihundert und mehr. Dadurch verändern die Bläschen von Aufnahme zu Aufnahme nur sehr wenig ihre Position. Sie lassen sich daher sehr viel einfacher nachverfolgen.
„Zusätzlich wollen wir in kommenden Studien einen speziellen Schallkopf nutzen, mit dem wir dreidimensionale Bilder erzeugen können“, sagt der Wissenschaftler. „Durch die Kombination dieser Maßnahmen können wir die Gefäße im Gehirn und ihren Zustand in sehr hoher Auflösung analysieren.“ Die Forscher haben kürzlich in einer Publikation in der Zeitschrift Stroke* veröffentlicht, welches Potenzial diese sogenannte Ultrasound Localization Microscopy hat.
In dem von der DEGUM geförderten Projekt wollen sie das Verfahren noch weiterentwickeln. Außerdem möchten sie untersuchen, inwiefern es sich zur schnellen Diagnose eines Schlaganfalls eignet. „Wir hoffen, dadurch auch früher Behandlungsschritte einleiten zu können, etwa um das verursachende Blutgerinnsel aufzulösen“, erläutert Regensburger.
Ein weiterer Schwerpunkt liegt auf der sogenannten Asphyxie, einem bedrohlichen Sauerstoffmangel nach der Geburt. Die Forschenden wollen zum Beispiel herausfinden, ob sie mit ihrer Methode die Hirngebiete sichtbar machen können, die besonders stark unter der Mangelversorgung leiden. Außerdem wollen sie untersuchen, wie das Gehirn auf die Notlage reagiert – ob es beispielsweise die Durchblutung der betroffenen Regionen erhöht und dafür die Versorgung anderer Bereiche herunterfährt. „Uns interessiert in diesem Zusammenhang auch, inwiefern wir aus Mechanismen wie diesen mögliche Therapiemaßnahmen ableiten können, um bleibende Schäden des Gehirns zu verhindern“, sagt der Mediziner.
*DOI: 10.1161/STROKEAHA.124.048390
Quelle: Friedrich-Alexander-Universität Erlangen-Nürnberg